Sản phẩm tăng cân G-Star và giảm cân L-Star chứa chất cấm Sibutramine, Phenolphthaleine?
Ngày 14/4/2011, Cục Quản lý Dược – Bộ Y tế đã có văn bản đình chỉ lưu hành và thu hồi toàn bộ sản phẩm chứa hoạt chất sibutramine. Đồng thời, trên website của cả Cục và Bộ này cũng đăng tải rất nhiều cảnh báo về tình trạng một số cá nhân vì lợi nhuận mà coi rẻ sức khỏe người tiêu dùng, vẫn để thành phần có chứa hoạt chất sibutramine và Phenolphthalein gây hại vào sản phẩm.
Các đơn vị Bộ Y tế cũng đã khuyến cáo rộng rãi về mức độ nguy hại của 2 hoạt chất Sibutramine và Phenolphthaleine đến sức khỏe con người như thế nào. Vậy nhưng trên thị trường hiện nay, sản phẩm tăng cân Viên bổ thảo mộc G-Star và sản phẩm viên giảm cân L-Star Original của Công ty TNHH Health Star có chứa chất cấm này nhưng vẫn được chào bán công khai.
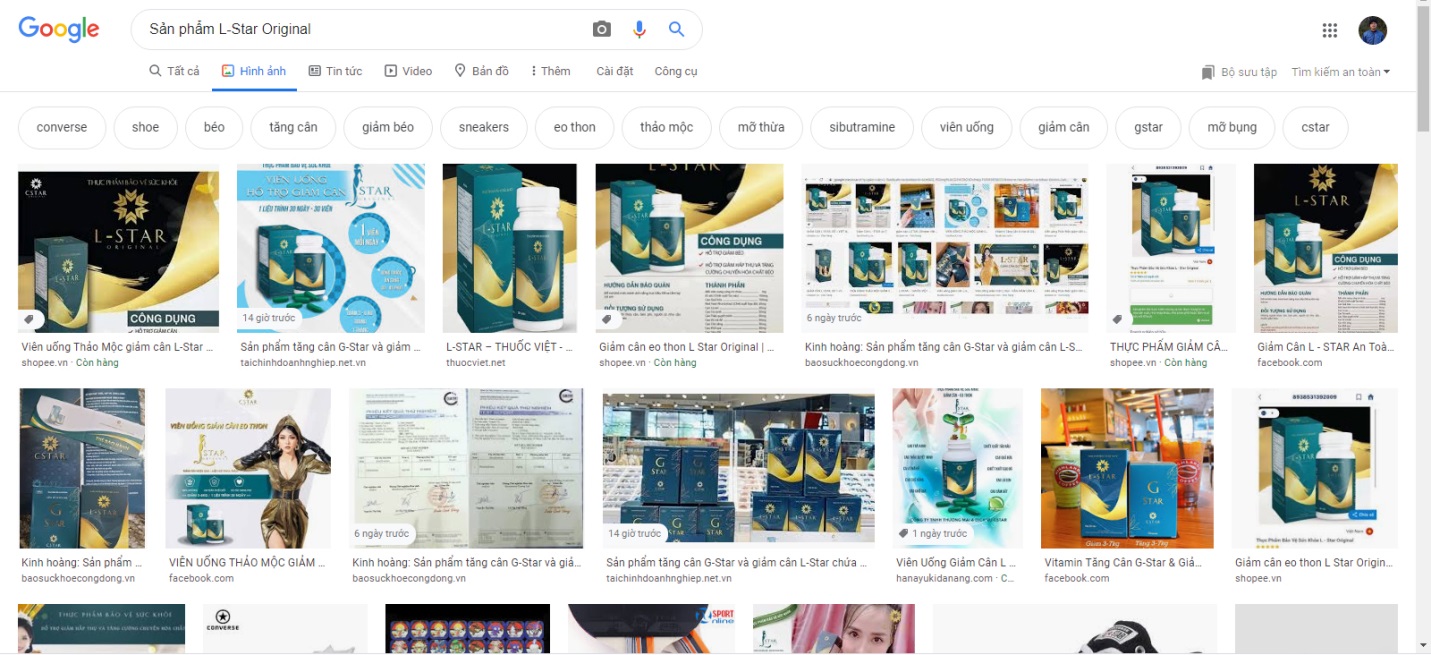
Sản phẩm Viên bổ thảo mộc G Star, L-Star Original chứa chất cấm bán tràn lan trên các kênh TMĐT và MXH.
Được biết, thuốc tăng cân G-Star, L-Star Original chính là phiên bản nâng cấp của viên uống tăng cân SQA gây sóng gió thị trường thời gian qua. Thông tin trên đã được xác nhận rộng rãi trên hệ thống phân phối sản phẩm thuốc tăng cân G-Star. Thuốc tăng cân G-Star được giới thiệu là siêu phẩm chuyên điều trị bệnh kém hấp thụ, gầy kinh niên, kém ăn, mất ngủ. Chỉ cần sử dụng 1 liệu trình là có thể đem lại những thay đổi rõ rệt trên cơ thể người bệnh.
Theo giới thiệu, 2 sản phẩm trên công dụng đặc trị giảm béo, tăng cân có giá được niêm yết: G-Star là 850.000 đồng và 950.000 đồng với viên giảm cân L-Star.

Các đơn vị chịu trách nhiệm về chất lượng sản phẩm, đơn vị phân phối và đơn vị sản xuất cùng số lô và số đăng ký sản phẩm được in trên bao bì.
Trên nhiều phương tiện truyền thông đều sử dụng giấy tiếp nhận đăng ký công bố sản phẩm số 13050/2019/ĐKSP ngày 30/11/2019, để minh chứng cho việc sản phẩm trên được công nhận bởi Bộ Y tế. Tuy nhiên, tìm kiếm trên website của Cục An toàn thực phẩm, Bộ Y tế thì không hề có thông tin gì về các sản phẩm G-Star và L-Star.
Theo tìm hiểu cũng như thông tin trên bao bì sản phẩm, viên bổ thảo mộc G-Star được phân phối bởi Công ty TNHH Thương mại & Dịch vụ C Star; còn viên uống giảm cân L-Star Original do Công ty TNHH Health Star phân phối và chịu trách nhiệm đưa sản phẩm ra thị trường . Tuy nhiên, hai công ty trên đều có cùng một địa chỉ đăng ký kinh doanh tại số 228 Lệ Ninh kéo dài, phường Quán Bàu, TP. Vinh, Nghệ An; với cùng 1 người đại diện pháp luật là bà Hoàng Thị Thuận.
Mặt khác, trên bao bì hộp sản phẩm của viên bổ thảo mộc G-Star thể hiện rõ mục thương nhân chịu trách nhiệm về sản phẩm lại là một đơn vị khác: Công ty TNHH Dược và Mỹ phẩm Anpha Gold, có địa chỉ tại số 47 Thanh Liệt, phường Thanh Liệt, Hoàng Mai, Hà Nội. Tuy nhiên, công ty này cũng có người đại diện theo pháp luật là bà Hoàng Thị Thuận.
Như vậy, qua tất cả các dữ liệu trên, có thể dễ dàng nhận thấy công ty chịu trách nhiệm về chất lượng sản phẩm và đơn vị phân phối hai dòng sản phẩm L-Star và G-Star đều cùng là một.
Đáng nói, theo thông tin kiểm nghiệm thành phần của 2 sản phẩm G-star và L-star Original từ Trung tâm Chứng nhận phù hợp (Quacert) cho thấy, trong thành phần của Viên bổ thảo mộc G-Star chứa hàm lượng chất Phenolphthalein; còn trong viên uống giảm cân L-Star Original chứa chất Sibutramine. Đây là hai hợp chất cấm - theo khuyến cáo của Bộ Y tế.
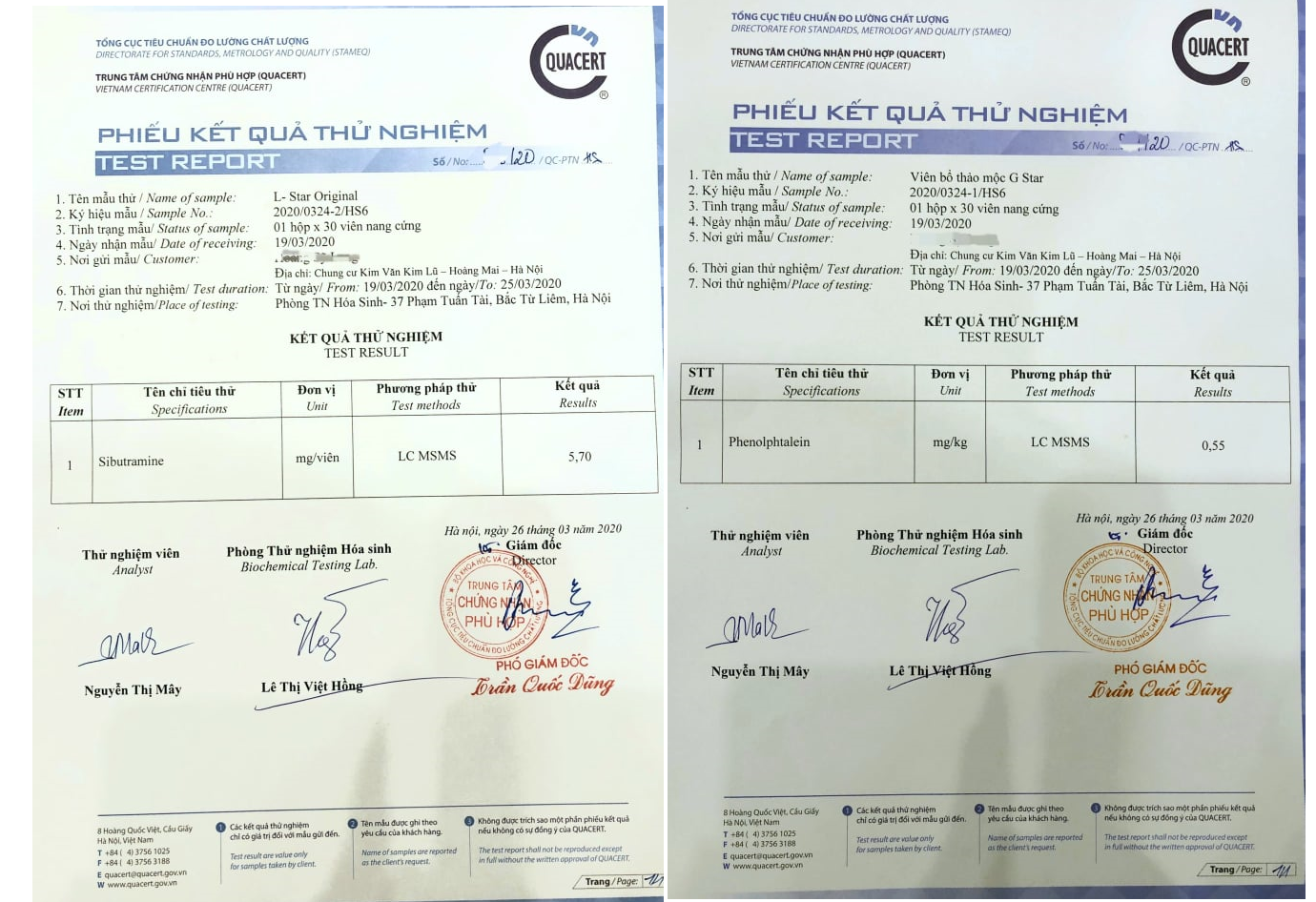
Phiếu kết quả kiểm nghiệm từ Trung tâm Chứng nhận phù hợp (Quacert) cho thấy 2 sản phẩm G-Star và L-Star có chứa chất cấm của Bộ Y Tế.
Qua tìm hiểu, Sibutramine là một hợp chất được sử dụng để giảm sự thèm ăn, thường được dùng trong điều trị bệnh béo phì. Hợp chất này được quản lý chặt chẽ và bị đưa ra khỏi thị trường vào tháng 10/2010 vì lý do an toàn.
Sản phẩm chứa chất này có thể gây hại cho người tiêu dùng vì có thể gây nên nguy cơ tăng huyết áp, tăng nhịp tim cho người bình thường và nguy hiểm cho những người có tiền sử bệnh về động mạch vành, đau tim, loạn nhịp tim hoặc đột quỵ. Sản phẩm này cũng có thể tương tác với các loại thuốc khác mà người dùng đang sử dụng, có thể dẫn đến nguy hiểm chết người.
Trong khi đó, Phenolphthalein là hóa chất thường được sử dụng trong việc đo độ kiềm/axit (pH) của dung dịch dựa vào khả năng đổi màu của nó. Chất này từng được sử dụng trong điều trị táo bón nhưng do các nghiên cứu cho thấy nó có khả năng là chất gây ung thư (carcinogen).
Vì vậy, Phenolphthalein đã được hạn chế và FDA cấm lưu hành các loại thuốc điều trị táo bón có chứa chất này mà bán không cần toa bác sĩ từ năm 1999. Theo thông tin từ FDA, hiện nay Phenolphthalein không có trong thành phần hoạt tính của bất cứ thuốc nào đang được sử dụng ở Mỹ.
Theo Nghị định 115 năm 2018 quy định xử phạt vi phạm hành chính về an toàn thực phẩm, ngoài xử phạt hành chính, có thể tước quyền sử dụng Giấy tiếp nhận đăng ký bản công bố sản phẩm tối đa lên tới 24 tháng. Trong một số trường hợp, nếu phát hiện những sai phạm có dấu hiệu hình sự, có thể chuyển cơ quan công an để điều tra.
Để thông tin khách quan hơn, PV đã liên hệ với Cục An toàn thực phẩm – Bộ Y tế và bà Hoàng Thị Thuận - đại diện pháp lý của Công ty TNHH Thương mại & Dịch vụ C Star và Công ty TNHH Health Star. Sức khỏe và Môi trường điện tử sẽ tiếp tục thông tin tới bạn đọc khi nhận được phản hồi.
Xuân Đoàn
Các tin khác

Trạm bơm tiêu Kim Xá - “Tan hoang” sau mùa bơm tiêu đầu tiên

Mường Ảng – Điện Biên: Nhiều dự án đầu tư công có dấu hiệu vi phạm các quy định pháp luật

Bài 2 (Hoài Đức, Hà Nội): Sự “vô cảm” của UBND xã Vân Canh trước hàng loạt tác động tiêu cực đang băm nát quy hoạch tại khu đô thị “ba không”

Chủ đầu tư thất hứa, đẩy dân vào thế khó

Bất chấp lệnh đình chỉ nhà hàng 173 Thái Hà “mở chui” đón khách

Xã Cảnh Hưng, Tiên Du, Bắc Ninh: Cuộc sống và sức khỏe của người dân đang bị ảnh hưởng bởi một bản án?

Vĩnh Phúc: Dự án nạo vét ao, hồ không đảm bảo gây ô nhiễm môi trường

Bình Thuận: Đất tặc lộng hành gây hệ lụy lớn

Hà Nội: Cần chấn chỉnh việc thi công “ẩu” gây ô nhiễm môi trường
Đọc nhiều

Danh sách những người trúng cử đại biểu HĐND TP Cần Thơ

Đắk Lắk: Cần thời gian để các lò gạch truyền thống chuyển đổi quy trình sản xuất mới

Cần Thơ khen thưởng Bệnh viện Đa khoa thành phố sau ca ghép thận đầu tiên thành công

Chuẩn hóa đội ngũ cán bộ, phường Ô Môn hướng tới chính quyền phục vụ

Cần Thơ: Bàn giao hệ thống xạ trị gia tốc cho Bệnh viện Ung bướu
Videos
E-magazine Inforgraphic Video

Nghi vấn xả thải ngầm khiến nguồn nước kênh mương tại xã Bình Minh (TP Hà Nội) ô nhiễm kéo dài

Thủ tướng động viên lực lượng bảo đảm vệ sinh môi trường ở Hà Nội

Diễn văn của Tổng Bí thư Tô Lâm tại phiên bế mạc Đại hội XIV của Đảng

Đại hội XIV của Đảng sự kiện trọng đại của đất nước trong giai đoạn mới

Hợp tác xã bệ đỡ vùng trồng rau an toàn tập trung tại Hưng Yên

Hưng Yên sản xuất rau quả công nghệ cao hướng đi bền vững cho nông nghiệp sạch

Xã Ô Diên – Hà Nội: Bất cập từ bãi vật liệu xây dựng gây ô nhiễm môi trường và trách nhiệm quản lý tại địa bàn cơ sở

Cảnh báo hành vi giả danh cán bộ thuế, cơ quan thuế để lừa đảo

Công an phường Long Biên, Hà Nội xử lý nghiêm xe chở đất gây ô nhiễm

Bắc Ninh: Tưng bừng khai hội Đền Đô năm 2026

Sôi động du lịch Cần Thơ, các điểm sinh thái hút khách dịp lễ

Cà Mau kỷ niệm 80 năm Trận Giồng Bốm, tri ân và phát huy truyền thống

Herbalife Việt Nam tham dự chương trình cộng đồng Mỹ-ASEAN

MEYGROUP tổ chức Lễ khai trương Văn phòng Bán hàng & Trải nghiệm Meyhomes Capital Phú Quốc

Vietjet đứng đầu Đông Nam Á về tối ưu phát thải trên các chuyến bay nội vùng

Vietjet và SPDB Financial Leasing ký kết thoả thuận tài trợ thuê mua 10 tàu bay Comac

Thủ tướng đề xuất 3 ưu tiên chiến lược cho 3 chuyển động lớn của thế giới

Nhiều chương trình hấp dẫn đón Xuân Ất Tỵ tại Cantho Eco Resort

Trung Quốc: Số ca mắc bệnh lý đường hô hấp tiếp tục tăng

Báo động tỷ lệ nhiễm HIV ở phụ nữ và trẻ em gái

Chuyên gia gỡ “nút thắt” về pháp lý, truyền thông cho cơ sở y tế ngoài công lập trong giai đoạn mới của thị trường

Bệnh viện Quân y 121 kiểm tra công tác phòng, chống say nắng, say nóng, phòng chống dịch bệnh

Nước hoa, mỹ phẩm cao cấp UNI: Tinh hoa từ Trầm Hương Việt

Bác sĩ Trần Nguyên Giáp: Chuyện “dính phốt” của một người quá mát tay trong ngành thẩm mỹ

Hội thảo khoa học về vết thương mạn tính: hướng đến giải pháp điều trị toàn diện, bền vững

VUSTA - Hành trình 43 năm bền bỉ kiến tạo và cống hiến
Chiến lược phát triển, ứng dụng năng lượng nguyên tử vì mục đích hòa bình

Thủ tướng: Phụ nữ Việt Nam vượt qua chính mình, trở thành lực lượng nòng cốt, nhân tố kiến tạo tiến trình đổi mới và phát triển
Nổi bật

Công an phường Long Biên, Hà Nội xử lý nghiêm xe chở đất gây ô nhiễm

Bắc Ninh: Tưng bừng khai hội Đền Đô năm 2026

Sôi động du lịch Cần Thơ, các điểm sinh thái hút khách dịp lễ

Đắk Lắk kích cầu du lịch dịp lễ 30/4 – 1/5: Kết nối văn hóa biển, nâng cao trải nghiệm xanh

Đính chính thông tin khỉ tấn công du khách: Cần nhìn đúng để bảo đảm an toàn và môi trường du lịch

Hơn 30 chuyên gia từ Mỹ và Anh khám từ thiện cho bệnh nhân nghèo

TTYT huyện Yên Lạc: Đẩy mạnh cải cách hành chính hướng tới sự hài lòng người bệnh
Bệnh viện C Thái Nguyên: Nghiên cứu và ứng dụng khoa học, kỹ thuật trong công tác khám, chữa bệnh

Bệnh viện Lao và bệnh Phổi Thái Nguyên nỗ lực vượt mọi khó khăn trong khám và điều trị bệnh

Trung tâm Y tế thị xã Phổ Yên: Nơi người bệnh gửi gắm niềm tin

Bệnh viện A Thái Nguyên: Nỗ lực, cống hiến, vì sức khỏe nhân dân

Trung tâm y tế huyện Đồng Hỷ: Nâng cao chất lượng chăm sóc và bảo vệ sức khỏe nhân dân
Trung tâm Y tế Chợ Đồn (Bắc Kạn): Không ngừng đổi mới, nâng cao chất lượng khám chữa bệnh